Trypanosoma cruzi
| Trypanosoma cruzi | |
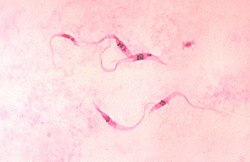 Trypanosoma cruzi, crithidia | |
| Systematik | |
|---|---|
| Domän | Eukaryoter Eukaryota |
| Rike | Excavata |
| Stam | Euglenozoa |
| Klass | Kinetoplastida |
| Ordning | Trypanosomatidae |
| Släkte | Trypanosoma |
| Art | Trypanosoma cruzi |
| Vetenskapligt namn | |
| § Trypanosoma cruzi | |
| Auktor | Chagas, 1909 |
Trypanosoma cruzi är en encellig, parasitisk eukaryot (protozo) som enligt Arbetsmiljöverket har riskklass 3. Detta innebär att den klassas som ett smittämne med risk för allvarliga konsekvenser vid exponering.[1] Infektion av Trypanosoma cruzi är kronisk och en minoritet av de som bär på parasiten utvecklar Chagas sjukdom, ett sjukdomstillstånd som kan leda till döden.
Trypanosoma cruzi är en zoonos som kan överföras mellan däggdjur och människor via blodsugande insekter, en slags rovskinnbaggar (Reduviidae) i underfamiljen Triatomine. Människor som lever under primitiva förhållanden, trångt och smutsigt, riskerar dock att bli smittade av infekterade insekter. Dessa insekter suger blod från människan och domesticerade husdjur och producerar sedan avföring som är infekterad med parasiten. Sedan förs parasiten vidare genom att avföringen kommer i kontakt med sår på hud eller slemhinnor. Smittan kan även ske vid blodtransfusioner, organdonationer eller genom förtäring av mat som har blivit kontaminerad med avföring från infekterade insekter.[2][3][4]
Historia
Den första dokumentationen av Trypanosoma cruzi gjordes 1909 av Carlos Riberiro Justiniano Chagas, en brasiliansk läkare som först beskrev Chagas sjukdom.[5]
Historiskt sett har spridning och dödsfall kopplade till parasiten varit begränsade till den Latinamerikanska landsbygden där undermåliga levnadsförhållanden utgjorde goda förutsättningar för vektorer att frodas. De senaste årtiondena har dock framgångsrik bekämpning av ohyra lett till en minskning av parasiten på landsbygden men migration inom landet har istället lett till en spridning till städer både inom och utanför Latinamerika.
Sedan 1991 har stora ansträngningar gjorts för att minska förekomsten av vektorer i bostäder och 2007 bildades ett initiativ i Latinamerika vars syfte var att uppmärksamma globaliseringen av Chagas sjukdom som uppstått på grund av att smittan spridits med resenärer mellan kontinenterna. Trots de ansträngningar som gjorts räknas det med att 8 miljoner till 16-18 miljoner människor över hela världen redan har blivit smittade av Trypanosoma cruzi vilket innebär att Chagas sjukdom kommer att finnas kvar i årtionden framöver.[6][7]
Evolution
Man vet inte säkert hur Trypanosoma cruzi har evolverat fram till dagens art men den kanske vanligast förekommande uppfattningen är att parasiten härstammar från en artrikare gren av trypanosomer som var specialiserade på fladdermöss. Enligt teorin ska dessa ha evolverat i fladdermössen för att sedan ta sig över till andra däggdjur. Ett alternativ till teorin är att föregångaren till Trypanosoma cruzi evolverade i fladdermöss för att sedan kunna infektera endast landlevande däggdjur. Det skulle kunna förklara den förvånansvärt sena men snabba spridningen av Chagas sjukdom hos människan.[8]
Forskare världen över har länge trott att Trypanosoma cruzi förökas klonalt och det är fortfarande vad man tydligast visat. Dock så har nyare studier visat tecken på rekombination och genetisk selektion. I vissa fall har man till och med kunnat utesluta direkt klonal överföring av gener.[9] Gener som man har visat påverkas av positiv selektion är loci som kodar för försvarsmekanimser mot värdens immunförsvar samt egenskaper som skulle kunna skydda patogenen från eventuellt framtida mediciner eller vaccin.[10]
Livscykel

I sin vektor återfinns Trypanosoma cruzi i två olika former. Parasiten överförs vid blodsugning och är då en rörlig metacyklisk trypomastigot. Väl inne i insektens matkanal omvandlas den till en epimastigot, vilket är parasitens replikationsstadium i vektorn. Efter delning tar den sig vidare till slutet av mag-tarmkanalen och omvandlas återigen till en metacyklisk trypomastigot.[2][11]
Då den smittade vektorn suger blod från ett däggdjur, exempelvis människa, bildas små sår. Genom såren kan insektens avföring, som innehåller trypomastigoter, komma in om värddjuret kliar sig till följd av bettet. Parasiten hamnar då i däggdjurets blodomlopp. En del av trypomastigoterna ligger kvar i blodomloppet och väntar på att en ny skinnbagge ska komma med nya spridningsmöjligheter. De allra flesta tar sig dock in i kroppscellernas cytoplasma för att utvecklas till amastigoter. I detta stadium är parasiten orörlig och delar sig obehindrat till dess att det inte får plats fler inne i cellen. Då omvandlas amastigoterna till rörliga trypomastigoter igen och frisätts till blodbanan då cellen spruckit till följd av att den överfyllts med patogener. Parasiten kan då ta sig in i en ny cell för att påbörja replikation på nytt, alternativt infektera en ny blodsugande vektor. Utan behandling pågår replikations-processen i värddjurets celler resten av dess liv, därför leder infektion till kroniska sjukdomstillstånd.[11][12]
Sjukdomar orsakade av Trypanosoma cruzi sprids framförallt från vektor till människa men kan även smitta mellan två människor vid blodtransfusion samt från mor till barn under graviditet.[13]
Referenser
- ^ Arbetsmiljöverket, (2014). Mikrobiologiska arbetsmiljörisker - smitta, toxinpåverkan, överkänslighet, [online] ”Arkiverade kopian”. Arkiverad från originalet den 28 juli 2014. https://web.archive.org/web/20140728092129/http://www.av.se/dokument/afs/afs2005_01.pdf. Läst 28 juli 2014., hämtad 15-04-11
- ^ [a b] Kirchhoff, L.V. (2014). Chagas Disease (American Trypanosomiasis). [online] http://emedicine.medscape.com/article/214581-overview, hämtad 2015-04-21
- ^ Xavier, S.C.D.C.; Roque, A.L.R.; Bilac, D.; de Araujo, V.A.L.; Neto, F.C.; Lorosa, E.S.; da Silva, L.F.C.F; Jansen, A.M. (2014). Distantiae Transmission of Trypanosoma cruzi: A New Epidemiological Feature of Acute Chagas Disease in Brazil. PLOS Neglected Tropical Diseases. 8(5): e2878. doi:10.1371/journal.pntd.0002878
- ^ Santana, R.A.G..; Guerra, M.G.V.B.; Sousa, D.R.; Couceiro, K.; Ortiz, J.V.; Oliveira, M.; Ferreira, L.S.; Souza, K.R.; Tavares, I.C.; Morais, R.F.; Silva, G.A.V.; Melo, G.C.; Vergel, G.M.; Albuquerque, B.C.; Arcanjo, A.R.L.; Monteiro, W.M.; Ferreira, J.M.B.B.; Lacerda, M.V.G.; Silveira, H.; Guerra, J.A.O. (2019). Oral Transmission of Trypanosoma cruzi, Brazilian Amazon. Emerging Infectious Diseases. (vol. 25) No:1 s. 132-133. DOI: https://doi.org/10.3201/eid2501.180646
- ^ World Health Organization, (2015). Chagas disease (American trypanosomiasis) [online] http://www.who.int/mediacentre/factsheets/fs340/en/, hämtad 15-04-21
- ^ National Center for Biotechnology Information, (2011). Trypanosoma cruzi and Chagas' Disease in the United States [online] http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3194829/, hämtad 15-04-21
- ^ Hemmige, V.; Tanowitz, H.; Sethi, A. (2012). Trypanosoma cruzi infection: a review with emphasis on cutaneous manifestations. International Journal of Dermatology. maj (vol. 51): s. 501-508. DOI: 10.1111/j.1365-4632.2011.05380.x
- ^ Hamilton, P.B.; Teixeira, M.M.G.; Stevens, J.R. (2012). Opinion: The evolution of Trypanosoma cruzi: the ‘bat seeding’ hypothesis. Trends in Parasitology. April (vol. 4): s. 136-141. DOI: 10.1016/j.pt.2012.01.006
- ^ Tomasini, N.; Lauthier, J.J.; Monje Rumi, M.M.; Ragone, P.G.; Alberti D'Amato, A.M.; Pérez Brandán, C.; Basombrío, M.A.; Diosque, P. (2014). Preponderant clonal evolution of Trypanosoma cruzi I from Argentinean Chaco revealed by Multilocus Sequence Typing (MLST). Infection, Genetics and Evolution. Oktober (vol. 27): s. 348-354. DOI: 10.1016/j.meegid.2014.08.003
- ^ Flores-López, C.A.; Machado, C.A. (2015). Differences in inferred genome-wide signals of positive selection during the evolution of Trypanosomacruzi and Leishmania spp. lineages: A result of disparities in host and tissue infection ranges? Infection, Genetics and Evolution. DOI: 10.1016/j.meegid.2015.04.008.
- ^ [a b] Walker, D.M.; Oghumu, S.; Gupta, G.; McGwire, B.S.; Drew, M.E.; Satoskar, A.R. (2014). Mechanisms of cellular invasion by intracellular parasites. Cellular and Molecular Life Sciences. April (vol. 71): s. 1245-1263. DOI: 10.1007/s00018-013-1491-1
- ^ Bern, C.; Kjos, S.; Yabsley, M.J.; Montgomery, S.P. (2011). Trypanosoma cruzi and Chagas' Disease in the United States. [online] http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3194829/, hämtad 2015-04-21
- ^ Läkare utan gränser. (2014). Chagas sjukdom. [online] http://www.lakareutangranser.se/chagas-sjukdom Arkiverad 26 april 2015 hämtat från the Wayback Machine., hämtad 2015-04-21
Externa länkar
 Wikimedia Commons har media som rör Trypanosoma cruzi.
Wikimedia Commons har media som rör Trypanosoma cruzi.
Media som används på denna webbplats
Trypanosoma forms in blood smear from patient with African trypanosomiasis. Trypanosoma forms in blood smear from patient with African trypanosomiasis. Parasite.
Trypanosomiasis, American [Trypanosoma cruzi]
An infected triatomine insect vector (or “kissing” bug) takes a blood meal and releases trypomastigotes in its feces near the site of the bite wound. Trypomastigotes enter the host through the wound or through intact mucosal membranes, such as the conjunctiva . Common triatomine vector species for trypanosomiasis belong to the genera Triatoma, Rhodinius, and Panstrongylus. Inside the host, the trypomastigotes invade cells, where they differentiate into intracellular amastigotes . The amastigotes multiply by binary fission and differentiate into trypomastigotes, and then are released into the circulation as bloodstream trypomastigotes . Trypomastigotes infect cells from a variety of tissues and transform into intracellular amastigotes in new infection sites. Clinical manifestations can result from this infective cycle. The bloodstream trypomastigotes do not replicate (different from the African trypanosomes). Replication resumes only when the parasites enter another cell or are ingested by another vector. The “kissing” bug becomes infected by feeding on human or animal blood that contains circulating parasites . The ingested trypomastigotes transform into epimastigotes in the vector’s midgut . The parasites multiply and differentiate in the midgut and differentiate into infective metacyclic trypomastigotes in the hindgut .
Trypanosoma cruzi can also be transmitted through blood transfusions, organ transplantation, transplacentally, and in laboratory accidents.
