Temperatur
| Den här artikeln behöver fler eller bättre källhänvisningar för att kunna verifieras. (2023-05) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. |
| Temperatur | |
| Grundläggande | |
|---|---|
| Alternativnamn | Termodynamisk temperatur |
| Definition | Förändring i inre energi av entropin |
| Storhetssymbol(er) | (för kelvin) (för grad Celsius) |
| Enheter | |
| SI-enhet | K, °C |
| SI-dimension | Θ |
| Planckenhet | Plancktemperatur |
| Planckdimension | ħ1/2·G−1/2·c5/2·k−1 |
| Astronomisk enhet | °F, °Ra |

Temperatur är en fysikalisk storhet och ett mått på värmetillstånd[1]. Värmeflödet är från en högre temperatur till en lägre temperatur. Vid lika temperatur är föremål i termisk jämvikt, se termodynamikens nollte huvudsats. Vidare kan också olika färgtoner av ljus mätas i så kallad färgtemperatur.
Definition
Temperatur definieras som förändringen i inre energi av entropin
där T är temperaturen i kelvin (K). Partiella derivatan, med volymen V och partikelantalet N fasta, är ofta en monotont växande funktion, vilket innebär att temperaturen alltid är positiv. Ett system har alltså låg temperatur om entropin ändras mycket när det tar upp värme. Värme flödar från ett system med hög temperatur till ett system med låg temperatur till dess att systemet som avger värme inte längre förlorar mer entropi på värmeförflyttningen än systemet som tar emot värme vinner. Då värmeflödet upphör har systemen tillsammans uppnått sin maximala entropi, temperaturen är lika och systemen befinner sig i termisk jämvikt med varandra.
Temperatur kan också beskrivas som den kinetiska energin i en ideal gas, det vill säga rörelsen hos molekylerna/atomerna inom ämnet. Vid högre temperatur rör de sig mer och vid lägre temperatur mindre.
Temperaturskalor

- Kelvinskalan – i vetenskapliga sammanhang används idag den absoluta skalan. Den har sin nollpunkt vid den temperatur som ett medium har då det är i sitt grundtillstånd (absoluta nollpunkten) och temperaturen uttrycks i enheten kelvin (K). Notera att kelvin inte inleds med en versal eftersom det tillhör SI-enheterna precis som meter, vilket skiljer den från övriga skalor i vilka ett temperaturområde delats in i steg (grader).
- Rankine – °R eller °Raa, som har samma steglängd som °F. Utgår från absoluta nollpunkten. Vatten fryser vid 491,67°R och kokar vid 671,64°R
Före den moderna uppfattningen om temperatur användes skalor med nollpunkten satt vid andra temperaturer än den absoluta nollpunkten. Av dem är följande fortfarande i allmänt bruk:
- Celsiusskalan – den vanligaste temperaturskalan i Sverige och globalt. Uppfunnen av svensken Anders Celsius. Temperaturer anges på skalan med enheten grad Celsius (°C), vars steglängd är lika med 1 K. Vatten fryser vid 0 °C och kokar vid 100 °C.
- Fahrenheitskalan – används i USA, Västindien och Liberia. Temperaturer anges på skalan med enheten grad Fahrenheit (°F). Vatten fryser vid 32 °F och kokar vid 212 °F.
Följande formler kan användas för att konvertera mellan temperaturerna T K, tC °C och tF °F:
- T = tC + 273,15
- tC = 5/9 · (tF − 32)
Äldre temperaturskalor som inte används längre
- Réaumur – °Ré, °Re eller °R. Steglängden är lika med 1,25 grader Celsius. Vatten fryser vid 0°Ré och kokar vid 80°Ré.
- Rømer – °Rø eller °R. Vatten fryser vid 7,5°Rø och kokar vid 60°Rø.
- Delisle – °De (stavas ibland de Lisle). Vatten fryser vid 150°De och kokar vid 0°De. Temperatur över kokpunkten räknas som minusgrader.
Omvandlingstabell
| Kelvin | Celsius | Fahrenheit | Rankine | Delisle | Newton | Réaumur | Rømer | Oktal | |
|---|---|---|---|---|---|---|---|---|---|
| Absoluta nollpunkten | 0 K | −273,15 °C | −459,67 °F | 0 °Ra | 549,73 °De | −90,14 °N | −218,52 °Ré | −135,9 °Rø | 0 |
| Vattnets fryspunkt | 273,15 K | 0 °C | 32 °F | 491,67 °Ra | 140 °De | 0 °N | 0 °Ré | 7,5 °Rø | 40 |
| Människans kroppstemperatur | 310,15 K | 37 °C | 98,6 °F | 558,27 °Ra | 94,5 °De | 12,21 °N | 29,6 °Ré | 26,93 °Rø | 44;25 |
| Vattnets kokpunkt | 373,15 K | 100 °C | 212 °F | 671,67 °Ra | 0 °De | 33 °N | 80 °Ré | 60 °Rø | 53;556 |
Se även
- Dolbears lag
- Lord Kelvin
- Negativ temperatur
- Operativ temperatur
- Rumstemperatur
- Termometer
- Väderrekord
Referenser
- ^ Svenska Akademiens ordböcker (SAOL, SO och SAOB) på Svenska.se: temperatur
Externa länkar
 Wikimedia Commons har media som rör Temperatur.
Wikimedia Commons har media som rör Temperatur.
| |||||
|
Media som används på denna webbplats
Författare/Upphovsman: Tkgd2007, Licens: CC BY-SA 3.0
A new incarnation of Image:Question_book-3.svg, which was uploaded by user AzaToth. This file is available on the English version of Wikipedia under the filename en:Image:Question book-new.svg
Författare/Upphovsman: unknown, Licens: CC BY-SA 3.0
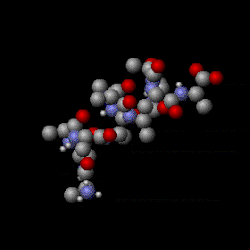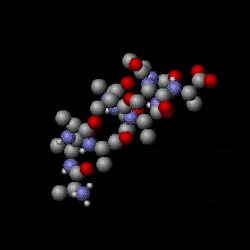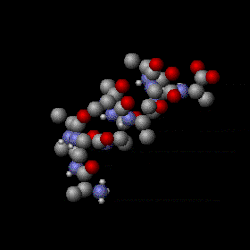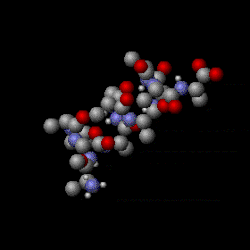
Shown here is the thermal motion of a segment of protein alpha helix. Molecules have various internal vibrational and rotational degrees of freedom. This is because molecules are complex objects; they are a population of atoms that can move about within a molecule in different ways. This makes molecules distinct from the noble gases such as helium and argon, which are monatomic (consisting of individual atoms). Heat energy is stored in molecules’ internal motions which gives them an internal temperature. Even though these motions are called “internal,” the external portions of molecules still move—rather like the jiggling of a water balloon.
Motion of gas molecules.
The randomized thermal vibrations of fundamental particles such as atoms and molecules—gives a substance its “kinetic temperature.” Here, the size of helium atoms relative to their spacing is shown to scale under 1950 atmospheres of pressure. These room-temperature atoms have a certain, average speed (slowed down here two trillion fold). At any given instant however, a particular helium atom may be moving much faster than average while another may be nearly motionless. The rebound kinetics of elastic collisions are accurately modeled here. If the velocities over time are plotted on a histogram, a Maxwell-Boltzmann distribution curve will be generated. Five atoms are colored red to facilitate following their motions.
Note that whereas the relative size, spacing, and scaled velocity of the atoms shown here accurately represent room-temperature helium atoms at a pressure of 1950 atmospheres, this is a two-dimensional scientific model; the atoms of gases in the real world aren’t constrained to moving in two dimensions in windows precisely one atom thick. If reality worked like this animation, there would be zero pressure on the two faces of the box bounding the Z-axis. The value of 1950 atmospheres is that which would be achieved if room-temperature helium atoms had the same inter-atomic separation in 3-D as they have in this 2-D animation.Författare/Upphovsman: 1-1111, Licens: CC BY-SA 3.0
Thermometer, dial pointer driven by a wound bi-metal



