Selendioxid
| Selendioxid | |
  | |
| Systematiskt namn | Selen(IV)oxid |
|---|---|
| Övriga namn | Selensyraanhydrid |
| Kemisk formel | SeO2 |
| Molmassa | 110,9588 g/mol |
| Utseende | Vita kristaller |
| CAS-nummer | 7446-08-4 |
| SMILES | O=[Se]=O |
| Egenskaper | |
| Densitet | 3,95 g/cm³ |
| Löslighet (vatten) | 384 g/l |
| Smältpunkt | 315 °C (sublimeras) |
| Faror | |
| Huvudfara | |
| SI-enheter & STP används om ej annat angivits | |
Selendioxid är en kemisk förening av selen och syre med formeln SeO2.
Egenskaper
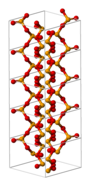
I fast form är selendioxid en polymer med omväxlande selen- och syre-atomer. I gasform antar det samma struktur som svaveldioxid. Selendioxid är giftigt och bildar selensyrlighet vid kontakt med vatten.
Framställning
Selendioxid kan framställas genom att oxidera selen genom förbränning i luft, med salpetersyra eller väteperoxid.
Användning
Selendioxid används för att färga glas rött eller för att balansera den blå färg som föroreningar av kobolt ger. Den ingår också i vissa blåneringsvätskor och som toner vid framkallning.
Se även
- Kiseldioxid
- Mangandioxid
- Tellurdioxid
Källor
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Selenium dioxide, tidigare version.
Media som används på denna webbplats
Symbol of pollutants to the environment, according to the directive 67/548/EWG of 'European Chemicals Bureau (European Chemicals Agency).
Ball-and-stick model chains in crystalline selenium dioxide, with unit cells displayed



