Rutherford-spridning
| Den här artikeln behöver källhänvisningar för att kunna verifieras. (2020-03) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. |
Rutherford-spridning innebär att laddade partiklar sprids från ett litet, massivt och laddat spridningscentrum.
I Ernest Rutherfords ursprungliga försök skickades alfapartiklar mot en guldfolie, varvid de spreds av guldatomerna. Analys av spridningsvinklar visade att en guldatoms laddning och massa är koncentrerad till ett litet område i dess mitt, atomkärnan, vilket visade att J. J, Thomsons atommodell inte stämde.
Externa länkar
Media som används på denna webbplats
Författare/Upphovsman: Tkgd2007, Licens: CC BY-SA 3.0
A new incarnation of Image:Question_book-3.svg, which was uploaded by user AzaToth. This file is available on the English version of Wikipedia under the filename en:Image:Question book-new.svg
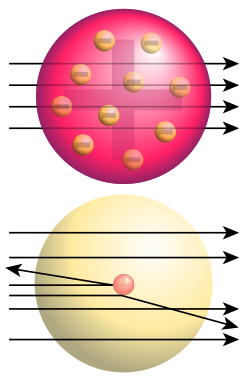
Top: Expected results of Rutherford's gold foil experiment: alpha particles passing through the plum pudding model of the atom undisturbed. Bottom: Observed results: Some of the particles were deflected, and some by very large angles. Rutherford concluded that the positive charge of the atom must be concentrated into a very small location: the atomic nucleus.