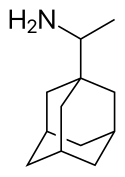
Rimantadin
| Rimantadin | |
  | |
| Systematiskt namn | (RS)-1-(1-adamantyl)etanamin |
|---|---|
| Kemisk formel | C10H15CH(NH2)CH3 |
| Molmassa | 179,302 g/mol |
| CAS-nummer | 13392-28-4 |
| SMILES | CC(N)C12CC3CC(C1)CC(C2)C3 |
| SI-enheter & STP används om ej annat angivits | |
Rimantadin är en organisk förening som är ett derivat av adamantan med formeln C10H15CH(NH2)CH3. Det är ett oralt administrerat antiviralt läkemedel[1] som används, dock sällan i Sverige, för att behandla och i sällsynta fall förebygga influensavirus A-infektion. När det tas inom ett till två dygn efter att symtomen har utvecklats, kan rimantadin förkorta varaktigheten och mildra svårighetsgraden av influensa. Rimantadine kan lindra symtom, inklusive feber.[2] Både rimantadin och det liknande läkemedlet amantadin är derivat av adamantan. Rimantadin har visat sig vara mer effektivt än amantadin eftersom patienten uppvisar färre symtom när det används.[3] Rimantadine godkändes av Food and Drug Administration (FDA) 1994.
Rimantadin godkändes för medicinskt bruk 1993.[4] Prover av säsongsbetonade H3N2 och 2009 års pandemiska influensa som testats har visat resistens mot rimantadin, och det rekommenderas inte längre att preparatet ordineras för behandling av denna typ av influensa. [5]
Medicinsk användning
Influensa A
Rimantadin hämmar influensaaktivitet genom att binda till aminosyror i M2-transmembrankanalen och blockera protontransport över M2-kanalen.[6] Rimantadin tros hämma influensans virusreplikation, möjligen genom att förhindra att virusets skyddande skal, som är höljet och kapsiden, avlägsnas. M2-kanalen är känd för att vara orsak till viral replikation i influensaviruset. Genetiska studier tyder på att virusets M2-protein, en jonkanal specificerad av virion M2-genen, spelar en viktig roll i känsligheten hos influensa A-virus för hämning av rimantadin.
Rimantadin är bundet inuti poren till amantadinspecifika aminosyrabindningsställen med väte- och van der Waals-bindningar.[7] Ammoniumgruppen (med närliggande vattenmolekyler) är placerad mot C-terminalen med amantadangruppen är placerad mot N-terminalen när den är bunden inuti M2-poren.

Influensaresistens
Resistens mot rimantadin kan uppstå som ett resultat av aminosyrasubstitutioner på vissa platser i transmembranregionen av M2. Detta förhindrar bindning av antiviral till kanalen.[8]
Mutations S31N-bindningsstället med rimantadin visas i bilden till vänster. Den visar rimantadinbindning till lumenala (överst) eller perifera (nedre) bindningsställen med influensa M2-kanal Serine 31 (guld) eller Asparagine 31 (blå).
Rimantadin enantiomer-interaktioner med M2
Rimantadin är, när det säljs som Flumadin, en racemisk blandning där både R- och S-tillstånden är ingår i läkemedlet. NMR-studier i fast tillstånd har visat att R-enantiomeren har en starkare bindningsaffinitet till M2-kanalporen än S-enantiomeren av rimantadin.[7] Eftersom enantiomererna har liknande bindningsaffinitet, har de också liknande förmåga att blockera kanalporen och fungera som en effektiv antiviral. Rimantadin-enantiomererna R och S är avbildade under interagerande med M2-poren nedan till höger. Denna bild visar ingen signifikant modellerad skillnad mellan R- och S-enantiomererna.
Parkinsons sjukdom
Rimantadin, liksom dess antivirala kusin amantadin, besitter vissa NMDA-antagonistiska egenskaper och kan användas vid behandling av Parkinsons sjukdom. I allmänhet är dock vare sig rimantadin eller amantadin ett föredraget medel för denna terapi och borde reserveras för fall av sjukdomen som är mindre känsliga för frontlinjebehandlingar.
Annat
Rimantadin har visat sig vara effektivt mot andra RNA-innehållande virus. Det kan behandla arbovirus som Saint Louis encefalit och Sindbis. Andra virus som kan behandlas med Rimantadin är respiratoriska syncytial och parainfluensavirus.[9] Rimantadin har också visat sig behandla kronisk hepatit C.[10]
Biverkningar
Rimantadine kan ge biverkningar i magtarmkanalen och centrala nervsystemet. Ungefär 6 procent av patienterna (jämfört med 4 procent av patienterna som fick placebo) rapporterade biverkningar vid en dos på 200 mg/d.[11] Vanliga biverkningar är:
- illamående
- orolig mage
- nervositet
- trötthet
- yrsel
- sömnsvårigheter (sömnlöshet)
- koncentrationssvårigheter
- förvirring
- ångest
Rimantadin visar färre CNS-symtom än systerläkemedlet Amantadin.[2]
Se även
Referenser
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Rimantadine, 30 november 2023.
Noter
- ^ Govorkova EA, Fang HB, Tan M, Webster RG (december 2004). ”Neuraminidase inhibitor-rimantadine combinations exert additive and synergistic anti-influenza virus effects in MDCK cells”. Antimicrobial Agents and Chemotherapy 48 (12): sid. 4855–63. doi:. PMID 15561867.
- ^ [a b] Zimmerman RK (mars 2007). ”Rationing of influenza vaccine during a pandemic: ethical analyses”. Vaccine 25 (11): sid. 2019–26. doi:. PMID 17258359.
- ^ Jefferson T, Demicheli V, Di Pietrantonj C, Rivetti D (april 2006). ”Amantadine and rimantadine for influenza A in adults”. The Cochrane Database of Systematic Reviews 2006 (2): sid. CD001169. doi:. PMID 16625539.
- ^ Long SS, Pickering LK, Prober CG (2012) (på engelska). Principles and Practice of Pediatric Infectious Disease. Elsevier Health Sciences. sid. 1502. ISBN 978-1437727029. https://books.google.com/books?id=nQ7-o8JAH7kC&pg=PA1502
- ^ Antiviral Agents for the Treatment and Chemoprophylaxis of Influenza: Recommendations of the Advisory Committee on Immunization Practices (ACIP)
- ^ Vorobjev YN (april 2020). ”An effective molecular blocker of ion channel of M2 protein as anti-influenza A drug.”. Journal of Biomolecular Structure and Dynamics 39 (7): sid. 2352–2363. doi:. ISSN 0739-1102. PMID 32212957.
- ^ [a b] Drakopoulos A, Tzitzoglaki C, Ma C, Freudenberger K, Hoffmann A, Hu Y, Gauglitz G, Schmidtke M, Wang J, Kolocouris A (februari 2017). ”Affinity of Rimantadine Enantiomers against Influenza A/M2 Protein Revisited”. ACS Medicinal Chemistry Letters 8 (2): sid. 145–150. doi:. PMID 28217261.
- ^ Jing X, Ma C, Ohigashi Y, Oliveira FA, Jardetzky TS, Pinto LH, Lamb RA (augusti 2008). ”Functional studies indicate amantadine binds to the pore of the influenza A virus M2 proton-selective ion channel”. Proceedings of the National Academy of Sciences of the United States of America 105 (31): sid. 10967–72. doi:. PMID 18669647.
- ^ Zlydnikov DM, Kubar OI, Kovaleva TP, Kamforin LE (1 maj 1981). ”Study of rimantadine in the USSR: a review of the literature”. Reviews of Infectious Diseases 3 (3): sid. 408–21. doi:. PMID 7025146.
- ^ Younossi ZM, Perrillo RP (1999). ”The roles of amantadine, rimantadine, ursodeoxycholic acid, and NSAIDs, alone or in combination with alpha interferons, in the treatment of chronic hepatitis C”. Seminars in Liver Disease 19 (Suppl 1): sid. 95–102. PMID 10349697.
- ^ ”CDC - Influenza (Flu) | Antivirals: Side-Effects | REMOVED!”. https://www.cdc.gov/flu/professionals/treatment/side-effects.htm. Läst 5 november 2008.
Externa länkar
 Wikimedia Commons har media som rör Rimantadin.
Wikimedia Commons har media som rör Rimantadin.
Media som används på denna webbplats
Författare/Upphovsman: Vaccinationist, Licens: CC BY-SA 4.0
Den här bilden skapades med Discovery Studio Visualizer.
Författare/Upphovsman:
Claire Scott1,2¤a, Jayakanth Kankanala2,3¤b, Toshana L. FosterID1,2¤c, Daniel H. GoldhillID4, Peng Bao5, Katie SimmonsID2,3, Marieke PingenID1¤d, Matthew Bentham1,2,
Elizabeth AtkinsID1,2¤e, Eleni LoundrasID1,2, Ruth Elderfield4¤f, Jolyon K. ClaridgeID6¤g, Joseph Thompson2,3¤h, Peter R. Stilwell4¤i, Ranjitha TathineniID1¤j, Clive S. McKimmieID1, Paul Targett-AdamsID7¤k, Jason R. SchnellID6, Graham P. Cook1, Stephen Evans5, Wendy S. Barclay4☯, Richard Foster2,3☯, Stephen GriffinID1,2*, Licens: CC BY-SA 4.0A visual model of rimantadine docking differences between the S31 and N31 mutation.