Kaliumklorat
| Kaliumklorat | |||||
 | |||||
| Systematiskt namn | Kaliumklorat | ||||
|---|---|---|---|---|---|
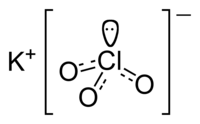
| Kemisk formel | KClO3 | ||||
| Molmassa | 122,55 g/mol | ||||
| Utseende | Vita kristaller eller vitt pulver | ||||
| CAS-nummer | 3811-04-9 | ||||
| SMILES | O=Cl(=O)[O-].[K+] | ||||
| Egenskaper | |||||
| Densitet | 2,34 g/cm³ | ||||
| Löslighet (vatten) | 71,9 g/l (20 °C) | ||||
| Smältpunkt | 356 °C | ||||
| Kokpunkt | 400 °C (sönderfaller) | ||||
| Faror | |||||
| Huvudfara |
| ||||
| NFPA 704 | |||||
| LD50 | 1870 mg/kg | ||||
| SI-enheter & STP används om ej annat angivits | |||||
Kaliumklorat, KClO3, är ett lättlösligt salt, som på grund av kloratjonens starkt oxiderande förmåga tillsammans med brännbara ämnen kan bilda explosiva blandningar.
Kaliumklorat brinner ej av sig själv. För detta krävs ett bränsle. I kombination med ett bränsle brinner blandningen med en svagt lila låga.
Framställning
Kaliumklorat kan framställas genom att leda klorgas genom en lösning av kaliumhydroxid. Metoden är dock ineffektiv eftersom det bildas fem gånger så mycket kaliumklorid som kaliumklorat.
Användningsområden
- I säkerhetständstickornas tändsats ingår kaliumklorat som ett oxidationsmedel (bildar syre till antändningsprocessen).
- I fotografiska sammanhang har kaliumklorat använts vid det så kallade platinaförfarandet, då man ville ha kontrastrika bilder.
- Kaliumklorat är en ingrediens i holländskt bad (Rembrandts etsvätska)
- Finlands armé använde kaliumklorat i Molotovcocktails under andra världskriget.
Media som används på denna webbplats
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for oxidizing substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Stuctural formula of potassium chlorate
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.








