Dimer
En dimer är en oligomer som består av två monomerer sammanfogade av bindningar som kan vara antingen starka eller svaga, kovalenta eller intermolekylära.[1] Dimerer har också stor betydelse i polymerkemi, oorganisk kemi och biokemi.
Termen homodimer används när de två molekylerna är identiska (till exempel A–A) och heterodimer när de inte är det (till exempel A–B). Det omvända till dimerisering kallas ofta dissociation. När två motsatt laddade joner förenas till dimerer, kallas de Bjerrum-par,[2] efter Niels Bjerrum.
Icke-kovalenta dimerer

Vattenfria karboxylsyror bildar dimerer genom vätebindning av det sura vätet och karbonylsyran. Till exempel bildar ättiksyra en dimer i gasfasen, där monomerenheterna hålls samman av vätebindningar.[3] Under speciella förhållanden bildar de flesta OH-innehållande molekyler dimerer, till exempel vattendimeren.
Excimerer och exciplexer är exciterade strukturer med kort livslängd. Ädelgaser bildar till exempel inte stabila dimerer, men de bildar excimererna Ar2*, Kr2* och Xe2* under högt tryck och elektrisk stimulering.[4]
Kovalenta dimerer

Molekylära dimerer bildas ofta genom reaktion av två identiska föreningar till exempel: 2A → A−A. I detta exempel sägs monomer "A" dimerisera för att ge dimeren "A−A ". Ett exempel är en diaminokarben, som dimeriserar för att ge en tetraaminoetylen:
Karbener är mycket reaktiva och bildar lätt bindningar.
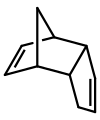
Dicyklopentadien är en asymmetrisk dimer av två cyklopentadienmolekyler som har reagerat i en Diels-Alder-reaktion för att ge produkten. Vid uppvärmning "spricker" den (genomgår en retro-Diels-Alder-reaktion) för att ge identiska monomerer:
Många icke-metalliska grundämnen förekommer som dimerer: väte, kväve, syre och halogenerna (det vill säga fluor, klor, brom och jod). Ädelgaser kan bilda dimerer kopplade av van der Waals-bindningar, såsom dihelium eller diargon. Kvicksilver förekommer som en kvicksilver(I)katjon (Hg2+2 formellt en dimerjon. Andra metaller kan bilda en andel dimerer i sin ångfas. Kända metalliska dimerer inkluderar dilitium (Li2), dinatrium (Na2), dikalium (K2), dirubidium (Rb2) och dicesium (Cs2) . Sådana elementära dimerer är homonukleära diatomiska molekyler.
Många små organiska molekyler, framför allt formaldehyd, bildar lätt dimerer. Dimeren av formaldehyd (CH2O) är dioxetan (C2H4O2) .
Boran (BH3) förekommer som dimer diboran (B2H6), på grund av den höga Lewis-surheten i borcentret.
Polymerkemi
I sammanhanget med polymerer hänvisar "dimer" också till polymerisationsgraden 2, oavsett stökiometri eller kondensationsreaktioner.
Ett fall där detta är tillämpligt är med disackarider. Till exempel är cellobios en dimer av glukos, även om bildningsreaktionen producerar vatten:
Här har den resulterande dimeren en stökiometri som skiljer sig från det initiala paret av monomerer.
Disackarider behöver inte vara sammansatta av samma monosackarider för att betraktas som dimerer. Ett exempel är sackaros, en dimer av fruktos och glukos, som följer samma reaktionsekvation som presenterats ovan.
Aminosyror kan också bilda dimerer, som kallas dipeptider. Ett exempel är glycylglycin, som består av två glycinmolekyler förenade med en peptidbindning. Andra exempel är aspartam och karnosin.
Oorganiska dimerer
Grupp 13 dimerer
Boraner

Diboran (B2H6) är ett klassiskt exempel på en oorganisk dimer. Boran finns inte ensam som BH3, även om det ofta skrivs på det sättet. B2H6 existerar som en struktur där två väteatomer överbryggar de två boratomerna. De överbryggande BH-bindningarna är lägre i bindningsordning än vad som skulle förväntas för en vanlig BH-bindning (de har lägre bindningsordning än de terminala BH-bindningarna). Detta förklaras av att bindningen har tre centra men bara två elektroner, "bananbindning", istället för den typiska enkelbindningen med två centra och två elektroner.[5]
Aluminium

Organoaluminiumkomplex kan existera som antingen monomerer eller dimerer baserat på den steriska massan av de bundna grupperna. Till exempel existerar metyl eller etylaluminium som en dimer, men när en mer skrymmande grupp tillsätts existerar komplexet som en monomer, såsom trimesitylaluminium.[6]
Biokemiska dimerer
Pyrimidindimerer
Pyrimidin-dimerer (även kända som tymindimerer) bildas genom en fotokemisk reaktion från pyrimidin-DNA-baser när de utsätts för ultraviolett ljus.[6] Denna tvärbindning orsakar DNA-mutationer, som kan vara cancerframkallande och orsaka hudcancer.[6] När pyrimidindimerer är närvarande kan de blockera polymeraser, vilket minskar DNA-funktionaliteten tills den är reparerad.[6]
Proteindimerer

Proteindimerer uppstår från interaktionen mellan två proteiner som kan interagera ytterligare för att bilda större och mer komplexa oligomerer.[7] Till exempel bildas tubulin genom dimerisering av α-tubulin och β-tubulin och denna dimer kan sedan polymerisera ytterligare för att göra mikrotubuli.[8] För symmetriska proteiner kan det större proteinkomplexet brytas ner i mindre identiska proteinsubenheter, som sedan dimeriseras för att minska den genetiska koden som krävs för att göra det funktionella proteinet.[7]
G-proteinkopplade receptorer
Som den största och mest mångsidiga familjen av receptorer inom det mänskliga genomet, har G-proteinkopplade receptorer (GPCR) studerats omfattande, med nya studier som stödjer deras förmåga att bilda dimerer.[9] GPCR-dimerer inkluderar både homodimerer och heterodimerer bildade från besläktade medlemmar av GPCR-familjen.[10] Även om det inte är alla, kräver vissa GPCR dimerisering för att fungera, såsom GABAB-receptor, vilket betonar vikten av dimerer i biologiska system.[11]

Receptortyrosinkinas
Ungefär som för G-proteinkopplade receptorer är dimerisering väsentlig för att receptortyrosinkinaser (RTK) ska kunna utföra sin funktion i signaltransduktion, vilket påverkar många olika cellulära processer.[12] RTK existerar vanligtvis som monomerer, men genomgår en konformationsförändring vid ligandbindning, vilket gör att de kan dimerisera med närliggande RTK.[13][14] Dimeriseringen aktiverar de cytoplasmatiska kinasdomänerna vars uppgift är ytterligare signaltransduktion.[12]
Se även
Referenser
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Dimer (chemistry), 3 mars 2023.
Noter
- ^ ”Dimer”. Illustrated Glossary of Organic Chemistry. UCLA. https://www.chem.ucla.edu/~harding/IGOC/D/dimer.html.
- ^ Adar, Ram M.; Markovich, Tomer; Andelman, David (2017-05-17). ”Bjerrum pairs in ionic solutions: A Poisson-Boltzmann approach”. The Journal of Chemical Physics 146 (19): sid. 194904. doi:. ISSN 0021-9606. PMID 28527430. Bibcode: 2017JChPh.146s4904A.
- ^ Karle, J.; Brockway, L. O. (1944). ”An Electron Diffraction Investigation of the Monomers and Dimers of Formic, Acetic and Trifluoroacetic Acids and the Dimer of Deuterium Acetate 1” (på engelska). Journal of the American Chemical Society 66 (4): sid. 574–584. doi:. ISSN 0002-7863. https://pubs.acs.org/doi/abs/10.1021/ja01232a022.
- ^ Birks, J B (1975-08-01). ”Excimers”. Reports on Progress in Physics 38 (8): sid. 903–974. doi:. ISSN 0034-4885. https://iopscience.iop.org/article/10.1088/0034-4885/38/8/001.
- ^ Shriver, Duward (2014) (på english). Inorganic Chemistry (6th). W.H. Freeman and Company. sid. 306–307. ISBN 9781429299060
- ^ [a b c d] Shriver, Duward (2014) (på english). Inorganic Chemistry (6th). W.H. Freeman and Company. sid. 377–378. ISBN 9781429299060
- ^ [a b] Marianayagam, Neelan J.; Sunde, Margaret; Matthews, Jacqueline M. (2004). ”The power of two: protein dimerization in biology”. Trends in Biochemical Sciences 29 (11): sid. 618–625. doi:. ISSN 0968-0004. PMID 15501681. http://dx.doi.org/10.1016/j.tibs.2004.09.006.
- ^ Cooper, Geoffrey M. (2000). ”Microtubules” (på engelska). The Cell: A Molecular Approach. 2nd Edition. https://www.ncbi.nlm.nih.gov/books/NBK9932/.
- ^ Faron-Górecka, Agata; Szlachta, Marta; Kolasa, Magdalena; Solich, Joanna; Górecki, Andrzej; Kuśmider, Maciej; Żurawek, Dariusz; Dziedzicka-Wasylewska, Marta (2019-01-01), Shukla, Arun K., red., ”Chapter 10 - Understanding GPCR dimerization” (på engelska), Methods in Cell Biology, G Protein-Coupled Receptors, Part B (Academic Press) 149: 155–178, doi:, ISBN 9780128151075, PMID 30616817, https://www.sciencedirect.com/science/article/pii/S0091679X18301080, läst 27 oktober 2022
- ^ Rios, C. D.; Jordan, B. A.; Gomes, I.; Devi, L. A. (2001-11-01). ”G-protein-coupled receptor dimerization: modulation of receptor function” (på engelska). Pharmacology & Therapeutics 92 (2): sid. 71–87. doi:. ISSN 0163-7258. PMID 11916530. https://www.sciencedirect.com/science/article/pii/S0163725801001607.
- ^ Lohse, Martin J (2010-02-01). ”Dimerization in GPCR mobility and signaling” (på engelska). Current Opinion in Pharmacology. GPCR 10 (1): sid. 53–58. doi:. ISSN 1471-4892. PMID 19910252. https://www.sciencedirect.com/science/article/pii/S1471489209001672.
- ^ [a b] Hubbard, Stevan R (1999-04-01). ”Structural analysis of receptor tyrosine kinases” (på engelska). Progress in Biophysics and Molecular Biology 71 (3): sid. 343–358. doi:. ISSN 0079-6107. PMID 10354703.
- ^ Lemmon, Mark A.; Schlessinger, Joseph (2010-06-25). ”Cell Signaling by Receptor Tyrosine Kinases” (på english). Cell 141 (7): sid. 1117–1134. doi:. ISSN 0092-8674. PMID 20602996.
- ^ Lemmon, Mark A.; Schlessinger, Joseph; Ferguson, Kathryn M. (2014-04-01). ”The EGFR Family: Not So Prototypical Receptor Tyrosine Kinases” (på engelska). Cold Spring Harbor Perspectives in Biology 6 (4): sid. a020768. doi:. ISSN 1943-0264. PMID 24691965.
Externa länkar
 Wikimedia Commons har media som rör dimer.
Wikimedia Commons har media som rör dimer.
Media som används på denna webbplats
Författare/Upphovsman: Mehakk12, Licens: CC BY-SA 4.0
Ligand binding on receptor tyrosine kinase monomers promotes dimerization
Författare/Upphovsman: Jdtv, Licens: CC BY-SA 3.0
trimethylaluminium as its bridged dimer
Chemical structure of 1,2-dioxetane
Författare/Upphovsman: Nmkuhlman, Licens: CC BY-SA 3.0
A comparison of the chemical structures of Borane and Diborane






