Antocyanin


Antocyaniner (från grekiska ἄνθος ánthos, "blomma" och κυάνεος kyáneos, "blå") är glykosider av en typ av flavonoider kallade antocyanidiner. Den vanligaste konfigugrationen är en D-glukos bunden till position 3 på antocyanidinen, och dessa antocyaniner är därför 3-glukosider.[1] Vanliga övriga sockerarter som förekommer är, i fallande ordning, rhamnos, galaktos, xylos och arabinos. De vanligaste ingående antocyanidinerna, är cyanidin, delphinidin, pelargonidin, peonidin, petunidin och malvidin.[2][1]
Antocyaninerna är färgämnen (röda, blå eller violetta) hos många blomväxter och förekommer lösta i vätskan ("cellsaften") i vakuolerna. De ger växtens blommor, blad och frukt färg, till exempel hos blåklint och rosor, och de är också orsak till den röda färgen hos höstlövens blad när det gröna klorofyllet brutits ner (de gula färgerna orsakas främst av karotenoider). Antocyanin finns också i, bland annat, blåbär, blodapelsin, vinbär och druvorna som ger rödvin dess färg. Antocyaniner är inte de enda röda-blå färgämnena i växtvärlden och hos ordningen Caryophyllales finns "i deras ställe" betalainer.
Historik
I sin Die Farben der Blüthen ("Blommornas färger") benämner den tyske apotekaren Ludwig Clamor Marquart 1835 "det färgande ämnet i blå, violetta och röda [...] blommor" som Anthokyan och beskriver detta ämnes förekomst och egenskaper hos lösningar av det.[3] 1849 beskrev François Symphorien Morot (1820-1889) i Recherches sur la coloration des végétaux den första anlaysen av antocyanin (från blåklint), vilken visade att det bestod av kol, syre och väte och 1858 visade A. Glènard detsamma för antocyanin från rödvin. Större framsteg nåddes på 1910-talet då Richard Willstätter, Arthur Ernest Everest och andra kunde visa att färgen hos en mängd olika blommor kom från tre olika antocyaniner, att antocyaninerna var besläktade med flavonoler och andra flavonoider, samt att de innehöll socker.[4][5]
Biosyntes
Antocyaniner syntetiseras från en UDP-D-glukos och en antocyanidin med hjälp av enzymet antocyanidin-3-O-glukosyltransferas.[6][7] UDP-D-glukos syntetiseras i sin tur från UTP och D-glukos-6-fosfat (via D-glukos-1-fosfat).[8]
Användning
Utöver att de förekommer naturligt i många livsmedel används antocyaniner som livsmedelsfärgämnen (E163) bland annat i läskedrycker (t.ex. hallonsoda) och yoghurt. De fungerar som antioxidanter hos växterna och in vitro. Intag av exempelvis bär och frukter rika på antocyaniner anses därför kunna ha inverkan på kroppens försvar mot oxidativ stress, vilket anses vara viktigt exempelvis vid inflammationsprocesser.[9][10] Större epidemiologiska studier, som dokumenterat kostvanor under längre tid i relation till hälsa eller sjukdomar, har satt intag av antocyaniner i samband med flera positiva hälsoeffekter, dock har sådana studier begränsningar genom att ej kunna bevisa orsakssamband.[11][12] Absorption av antocyanidiner (dvs antocyaniner utan sockergrupp) i människans matsmältningskanal är dålig och de bryts snabbt ned och exkreteras.[13] Antocyaniners roll som antioxidanter för människor och djur har dock varit föremål för en rad studier och på senare tid har dos-responsstudier med antocyaniner genomförts,[14] men även studier som visat att bioaktiva metaboliter av antocyaniner kan förklara en del av effekterna. [15]
- De vanligaste antocyanidinerna
- Cyanidin
- Delphinidin
- Pelargonidin
- Peonidin
- Malvidin
- Petunidin
Referenser
- ^ [a b] Ibland binds en andra sockermolekyl till position 5 eller, sällsynt, till position 7. Vanligen är det monosackarider, men ibland disackarider eller trisackarider. Se European Food Safety Authority, 23 maj 2013, Scientific Opinion on the re-evaluation of anthocyanins (E 163) as a food additive Arkiverad 6 mars 2022 hämtat från the Wayback Machine., EFSA Journal 2013;11(4):3145, sid. 8.
- ^ Hock Eng Khoo, Azrina Azlan, Sou Teng Tang, See Meng Lim, 2017, Anthocyanidins and anthocyanins: colored pigments as food, pharmaceutical ingredients, and the potential health benefits, Food and Nutrition Research,61:1.
- ^ Ludwig Clamor Marquart, 1835, Die Farben der Blüthen, T Habicht, Bonn, sid. 55 ff.
- ^ Brenda S.J. Winkel, 2006, The Biosynthesis of Flavonoids, i Erich Grotewold (ed.), The Science of Flavonoids, sid. 73. ISBN 9780387288215.
- ^ Arthur Ernest Everest, 1914, The Production of Anthocyanins and Anthocyanidins, Proceedings of the Royal Society B, 87:597, sid. 444-452.
- ^ antocyanidin-3-O-glukosyltransferas på Brenda.
- ^ Anthocyanin Biosynthesis på International Union of Biochemistry and Molecular Biology.
- ^ UDP-glucose, UDP-galactose and UDP-glucuronate Biosynthesis på International Union of Biochemistry and Molecular Biology.
- ^ ”Arkiverade kopian”. Arkiverad från originalet den 14 maj 2012. https://web.archive.org/web/20120514050025/http://www.biolink.no/archive/anthocyanins-and-their-effect-on-chronic-inflammation-article25-29.html. Läst 14 december 2011.
- ^ http://www.nyfikenvital.org/?q=node/1900 Arkiverad 13 april 2014 hämtat från the Wayback Machine.
- ^ Cassidy, Aedín; Mukamal, Kenneth J.; Liu, Lydia; Franz, Mary; Eliassen, A. Heather; Rimm, Eric B. (2013-01-15). ”High anthocyanin intake is associated with a reduced risk of myocardial infarction in young and middle-aged women”. Circulation 127 (2): sid. 188–196. doi:. ISSN 1524-4539. PMID 23319811. PMC: 3762447. https://pubmed.ncbi.nlm.nih.gov/23319811/. Läst 2 april 2021.
- ^ Cassidy, Aedín; O'Reilly, Éilis J.; Kay, Colin; Sampson, Laura; Franz, Mary; Forman, J. P. (2011-02). ”Habitual intake of flavonoid subclasses and incident hypertension in adults”. The American Journal of Clinical Nutrition 93 (2): sid. 338–347. doi:. ISSN 1938-3207. PMID 21106916. PMC: 3021426. https://pubmed.ncbi.nlm.nih.gov/21106916/. Läst 2 april 2021.
- ^ Flavonoids på Linus Pauling Institute - Micronutrient Information Center: "In general, the bioavailability of flavonoids is low due to limited absorption, extensive metabolism, and rapid excretion. Isoflavones are thought to be the most bioavailable of all flavonoid subclasses, while anthocyanins and galloylated catechins are very poorly absorbed." och "... the relative contribution of dietary flavonoids to plasma and tissue antioxidant function in vivo is likely to be very small or negligible."
- ^ Xu, Zhongliang; Xie, Jiewen; Zhang, Hanyue; Pang, Juan; Li, Qing; Wang, Xu (2021-02). ”Anthocyanin supplementation at different doses improves cholesterol efflux capacity in subjects with dyslipidemia-a randomized controlled trial”. European Journal of Clinical Nutrition 75 (2): sid. 345–354. doi:. ISSN 1476-5640. PMID 32317748. https://pubmed.ncbi.nlm.nih.gov/32317748/. Läst 2 april 2021.
- ^ Rodriguez-Mateos, Ana; Istas, Geoffrey; Boschek, Lisa; Feliciano, Rodrigo P.; Mills, Charlotte E.; Boby, Céline (2019-06-18). ”Circulating Anthocyanin Metabolites Mediate Vascular Benefits of Blueberries: Insights From Randomized Controlled Trials, Metabolomics, and Nutrigenomics”. The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences 74 (7): sid. 967–976. doi:. ISSN 1758-535X. PMID 30772905. https://pubmed.ncbi.nlm.nih.gov/30772905/. Läst 2 april 2021.
Media som används på denna webbplats
Structure of cyanidin
chemical structure of peonidin
Petunidin
Cyanidin 3-O-glucoside; chrysontemin
Författare/Upphovsman:
- Indikator-Blaukraut.JPG: Supermartl
- derivative work: Haltopub (talk)
natural pH indicator Red Cabbage (left side acidic, right alkaline)
chemical structure of pelargonidin
chemical structure of malvidin
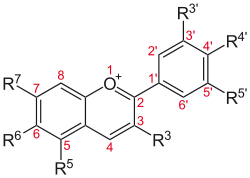
General structure of anthocyanidines














